【中心科研】Neurosci Bull丨魏磊/陆正齐/蔡蔚团队揭示阿戈美拉汀通过修复脑内“清道夫”系统,为帕金森病治疗提供新策略
帕金森病(PD)作为一种常见的神经退行性疾病,长期以来缺乏能够延缓疾病进展的有效手段。传统治疗多集中于缓解运动症状,而未能从根本上干预其病理进程。近年研究发现,脑内类淋巴系统(glymphatic system)功能障碍,尤其是水通道蛋白4(AQP4)在星形胶质细胞终足的极化失调,是导致α-突触核蛋白(α-syn)等毒性蛋白清除障碍的关键因素,也成为PD治疗的新靶点。
中山大学附属第三医院脑病中心神经内科魏磊副主任医师、陆正齐教授和蔡蔚副研究员团队,于2025年11月18日在Neuroscience Bulletin(JCR 1区)上发表重要研究,首次揭示抗抑郁及睡眠调节药物阿戈美拉汀 (Agomelatine,AGM)具有修复帕金森病患者和模型动物类淋巴系统功能的作用,并阐明其通过BMAL1-gap junction信号通路促进AQP4再极化的全新机制。该研究不仅拓展了阿戈美拉汀的临床应用前景,也为帕金森病的疾病修饰治疗提供了理论依据与实验支撑。

原文链接 https://link.springer.com/article/10.1007/s12264-025-01543-9
关键发现
在帕金森病中,作为大脑“清道夫系统”的类淋巴通路因AQP4蛋白在星形胶质细胞终足的极化紊乱而功能失调,导致α-syn等毒性废物无法有效清除,从而加速神经退化。该研究团队发现PD患者血浆褪黑素水平显著低于健康对照,且与类淋巴系统功能(基于DTI-ALPS指数的数据)呈正相关。AGM治疗3个月后,PD患者UPDRS运动评分显著降低,DTI-ALPS指数及PDSS评分显著升高,提示类淋巴系统引流功能及运动功能均得到改善。在MPTP诱导的PD小鼠模型中,AGM显著改善PD病理并恢复血管旁AQP4的极化,恢复脑内“清道夫”系统清除能力,其机制与已知的昼夜节律调节效应不同。转录组分析表明,AGM的作用可能涉及BMAL1介导的缝隙连接(gap junction)相关通路的上调。该研究首次揭示,常用睡眠调节药物阿戈美拉汀能够重塑类淋巴清除功能,不仅可以改善帕金森病患者运动症状与类淋巴引流障碍,还显著减轻PD小鼠多巴胺能神经元丢失与神经炎症,发挥了“对症”与“对因”治疗的双重作用。
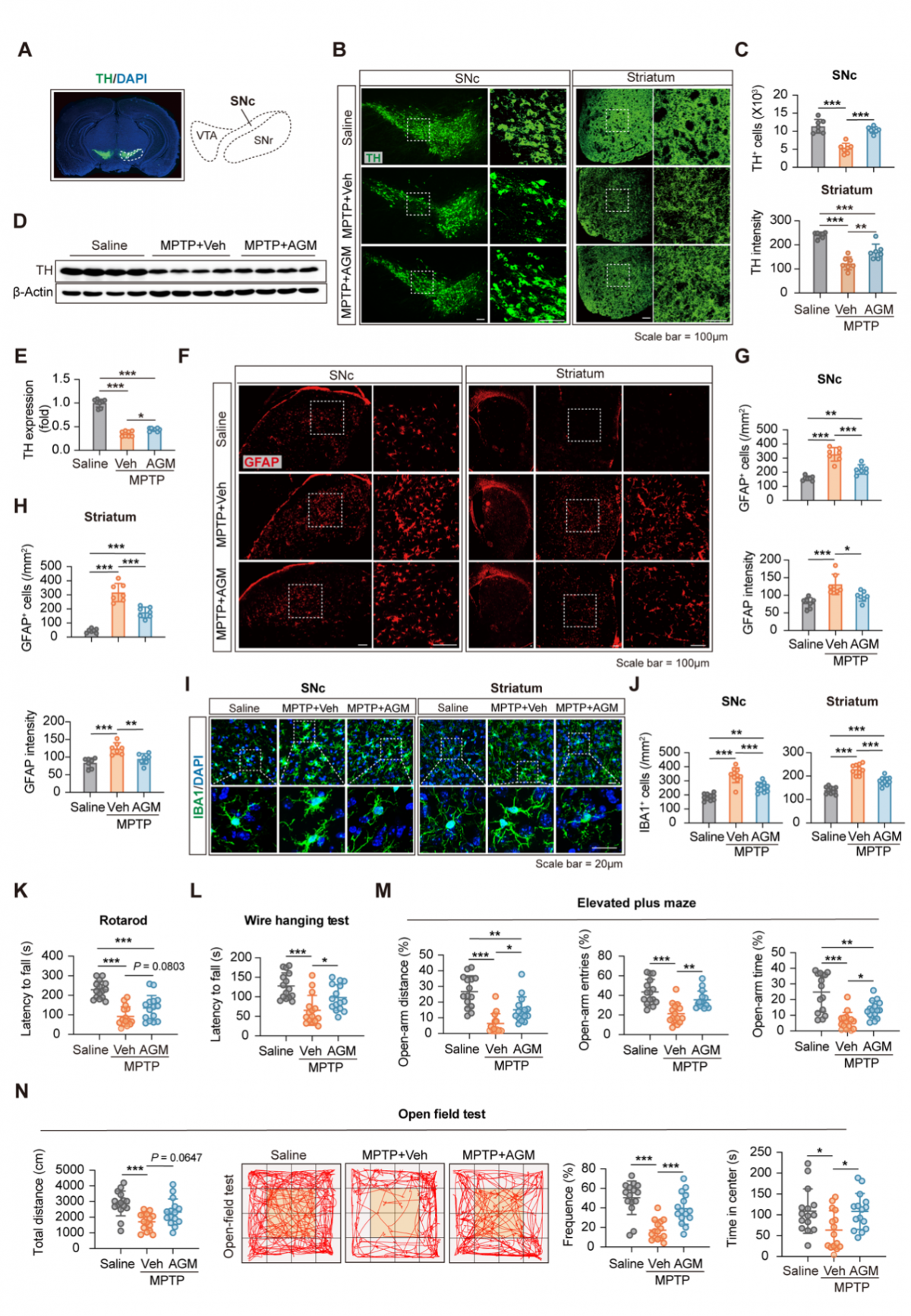
图1. AGM治疗改善了MPTP诱导的PD小鼠中的PD病理和焦虑样行为
未来展望
该研究首次揭示阿戈美拉汀通过调控生物钟—类淋巴—AQP4轴,成为一种兼具“症状改善”与“疾病修饰”双重潜力的帕金森治疗药物,实现了对蛋白清除障碍的底层干预。这一发现不仅为老药新用提供了理论依据,也为神经退行性疾病的疾病修饰治疗开辟了“调节内源性清除”的新范式。这一成果有望为众多帕金森病患者带来兼具症状改善与疾病延缓的双重获益。
研究团队
该研究由中山三院神经内科团队主导。魏磊副主任医师、陆正齐教授与蔡蔚副研究员担任通讯作者;王施思助理研究员、吴丹主管技师,陈国明医师为共同第一作者。










