我院皮肤与整形美容科朱蕾团队与清华大学徐弢团队通过生物3D打印技术构建预血管化人工皮肤,直面创面难愈及瘢痕愈合难题
皮肤作为人体最大的器官,是抵御外界损伤的重要屏障。然而在严重烧伤、糖尿病足、慢性溃疡等疾病中,皮肤的正常修复能力常常遭到破坏,导致创面长期无法愈合。对于这些难愈性创面患者来说,目前的治疗手段仍存在血供不足、细胞存活率低、组织结构重建困难等一系列瓶颈。特别是在创面形成的早期阶段,由于缺乏有效的血管网络支持,移植材料和干细胞常常难以在恶劣的微环境中长期存活,因此,构建能够“自带血供”,并具备三维组织结构和持续修复能力的皮肤替代物,成为再生医学领域亟待攻克的难题。
近日,我院皮肤与整形美容科朱蕾研究团队,在国际知名综合性期刊Advanced Science(中科院一区,IF=14.1)在线发表了题为“One-Step Coaxial 3D Printing of Pre-Vascularized Skin Organoid Models with ADSC Microspheres for Enhanced Wound Healing”的研究成果。该研究通过技术创新,将多种细胞、功能模块与可打印生物材料整合在同一体系中,为皮肤再生提供了结构更精细、功能更完善、并更贴近真实皮肤组织的新型工程化解决方案。
研究团队从临床需求出发,将 GelMA/Col1MA 作为可打印的真皮支架材料,同时引入含有脂肪来源干细胞(ADSCs)的微球结构,在支架内部构建岛状功能模块,让干细胞在三维空间内保持良好的活性与分布。更具突破意义的是,团队将血管内皮细胞与成纤维细胞共同嵌入打印体系中,使构建物在形成之初就具备预先组装的微血管网络,显著提升了移植后早期成活能力。这种“基质—微球—血管”共同参与的同轴打印方式,使研究人员能够通过一次打印完成复杂组织结构的构建,大幅提高了模型的稳定性与可控性。
研究利用一步式同轴 3D 打印技术,在水凝胶支架内部成功形成连续、稳定的预血管通道。内皮细胞在通道中迅速铺展并形成管腔,具备良好的形态结构和早期血管生成活性。该通道还呈现出类似天然微血管的通透性和细胞黏附特性,为构建物在移植后的快速血流接入奠定了基础。
同时,微流控技术制备的 ADSC 类器官微球在打印结构中呈岛状分布,保持高活性并持续释放修复因子,促进血管生成、成纤维细胞迁移和 ECM 重塑。动物实验显示,这些微球在整个创面愈合周期中均保持功能输出,显著加快创面闭合并提升再生皮肤质量。
在小鼠全层皮肤缺损模型中,预血管化皮肤类器官表现出显著的修复优势。移植后能更快接入宿主血供,加速创面闭合,并形成更接近正常皮肤的表皮与真皮结构。HE、Masson 及血管免疫染色均显示,该构建物可显著提高血管密度、促进胶原有序排列,减少瘢痕形成,整体修复质量远优于对照组。
此外,同轴 3D 打印体系能够灵活调节构建物的厚度、血管化程度及微球分布,实现对皮肤组织结构的高度可控构建。打印过程稳定、操作简便,可适配不同大小与形状的创面需求,为未来的大规模制备和临床推广奠定了技术基础。
我院硕士生王焜锐、蓝翔为论文共同第一作者,皮肤与整形美容科朱蕾、清华大学徐弢为共同通讯作者。我院为本论著的第一作者及通讯单位。

原文链接:https://advanced.onlinelibrary.wiley.com/doi/10.1002/advs.202517409
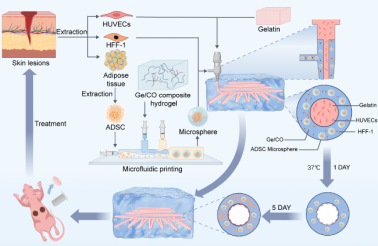
图1. 生物3D打印构建预血管化皮肤类器官模型(PV-SOM)的示意图
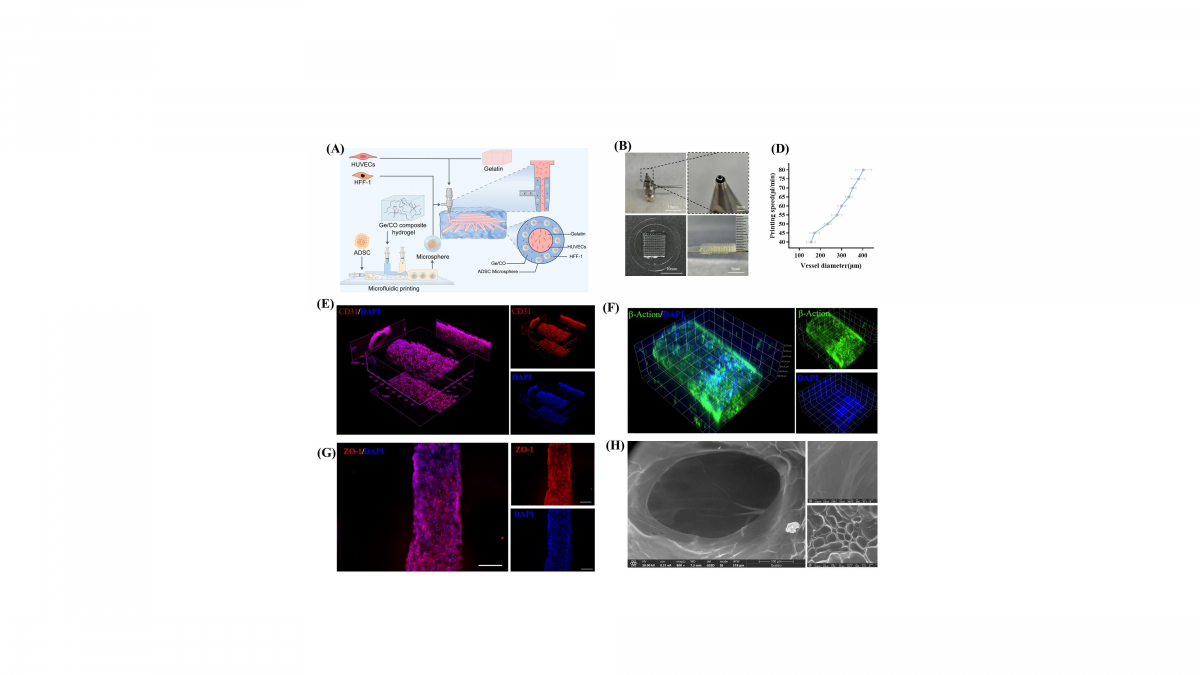
图2. 同轴 3D 打印构建出结构与功能完善的预血管通道
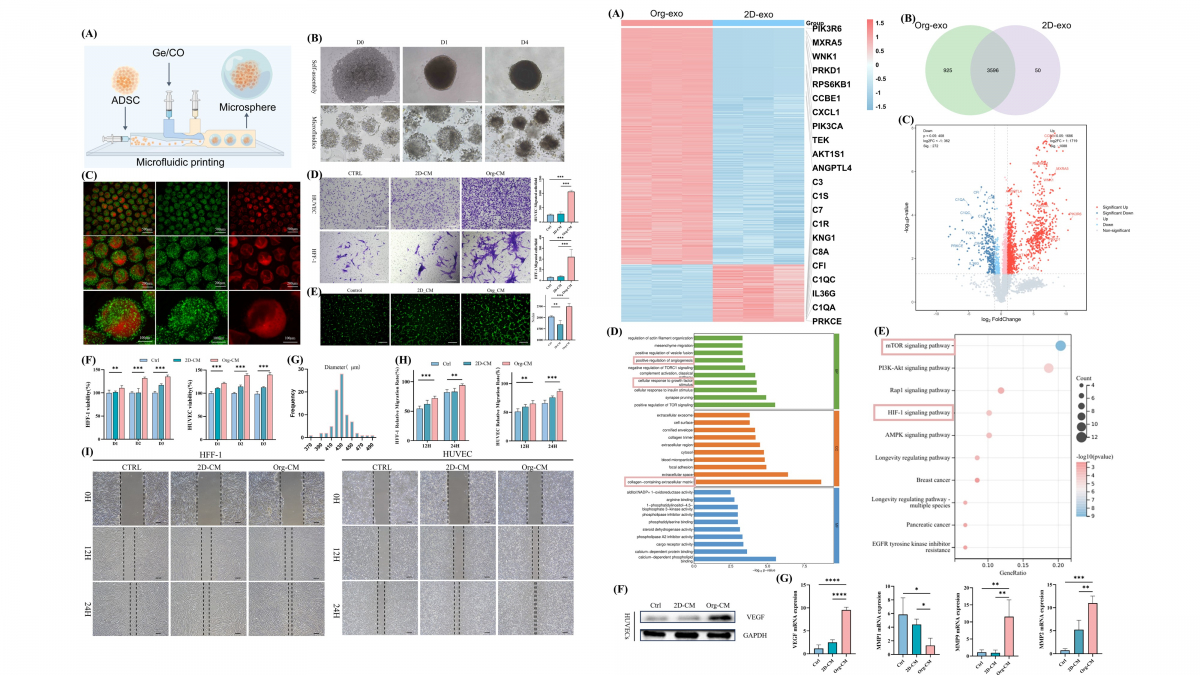
图3. ADSC 类器官微球,贯穿创面修复全程
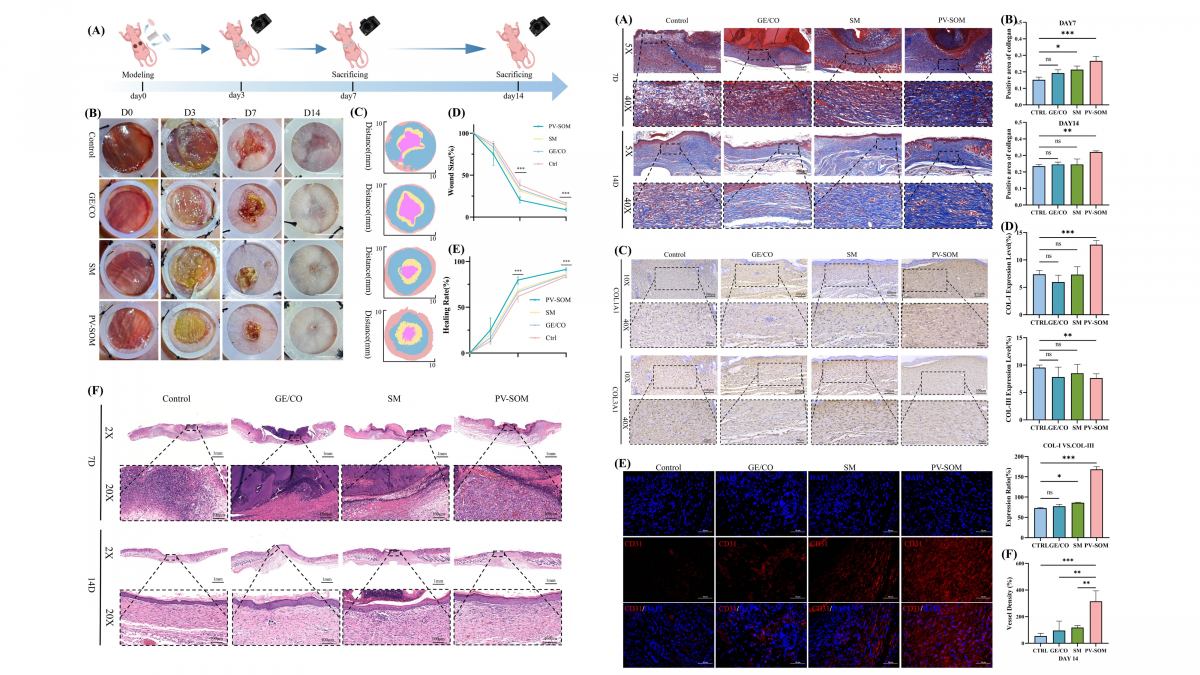
图4. PV-SOM显著促进创面愈合并提高再生质量
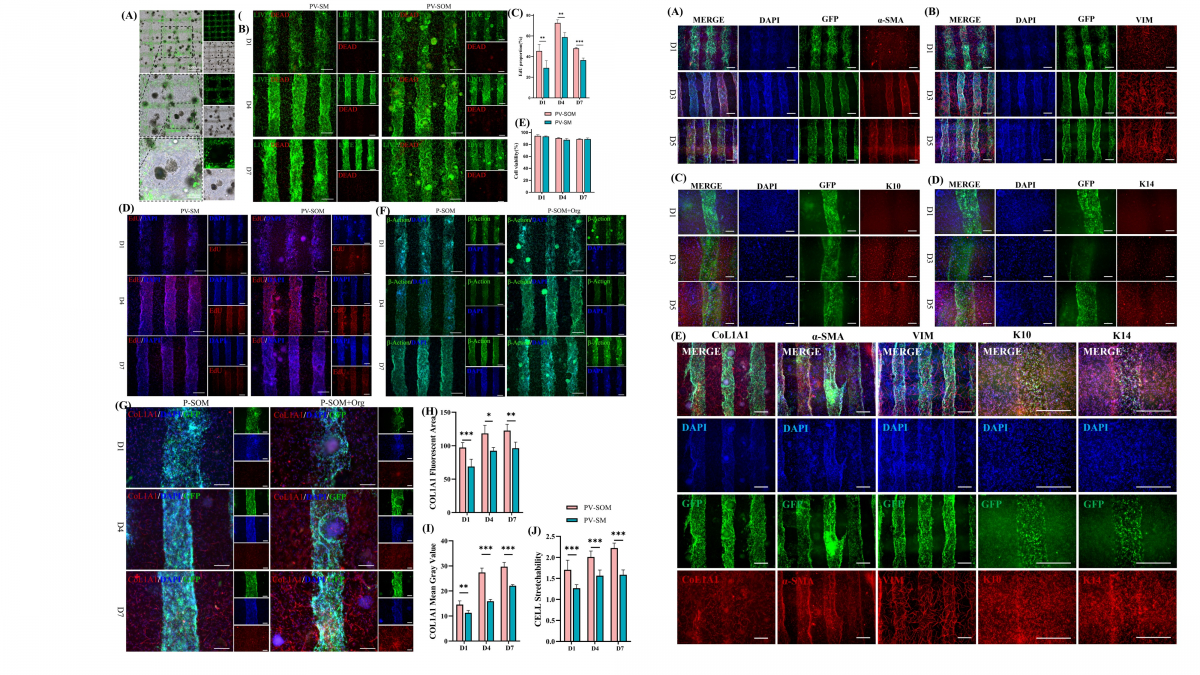
图5. PV-SOM可精准调控、结构可定制









