JCSM|我院彭晖教授团队发现肌-肾对话新机制:肌肉因子IL-15通过调控足细胞线粒体稳态改善糖尿病肾病
糖尿病肾病(DN)是全球终末期肾病(ESRD)的主要原因,其严重程度与足细胞损伤程度密切相关。越来越多的证据表明,高血糖诱导的线粒体功能障碍在足细胞损伤和DN发病机制中起到关键作用。骨骼肌作为内分泌器官,通过释放肌因子与远处器官进行交流,可能对肾脏产生保护作用。白细胞介素-15(IL-15)是一种主要由骨骼肌分泌的细胞因子,在调节代谢和线粒体功能方面发挥作用,但其在DN中对足细胞线粒体动力学的影响及机制尚未被探索。
我院彭晖教授团队与美国贝勒医学院Zhaoyong Hu教授合作在Journal of Cachexia, Sarcopenia and Muscle杂志(JCR Q1/中科院1区,IF:9.1)在线发表了题为“IL-15 Links Muscle-Kidney Crosstalk to Preserve Podocyte Mitochondrial Fusion and Attenuate Diabetic Nephropathy”的研究成果。该研究发现了肌肉因子IL-15通过维持足细胞线粒体融合来减轻糖尿病肾病,为糖尿病肾病提供了新的治疗方法。

为深入探究肌肉因子保护糖尿病肾脏的机制,研究团队构建了骨骼肌特异性过表达PGC-1α的转基因小鼠(mPGC-1α),并与db/db糖尿病小鼠杂交。研究发现,mPGC-1α:db/db小鼠表现出明显的肾脏保护效应---尿白蛋白排泄量、系膜基质扩张、肾小球基底膜增厚均显著减轻,足细胞数量得以保留(图1)。
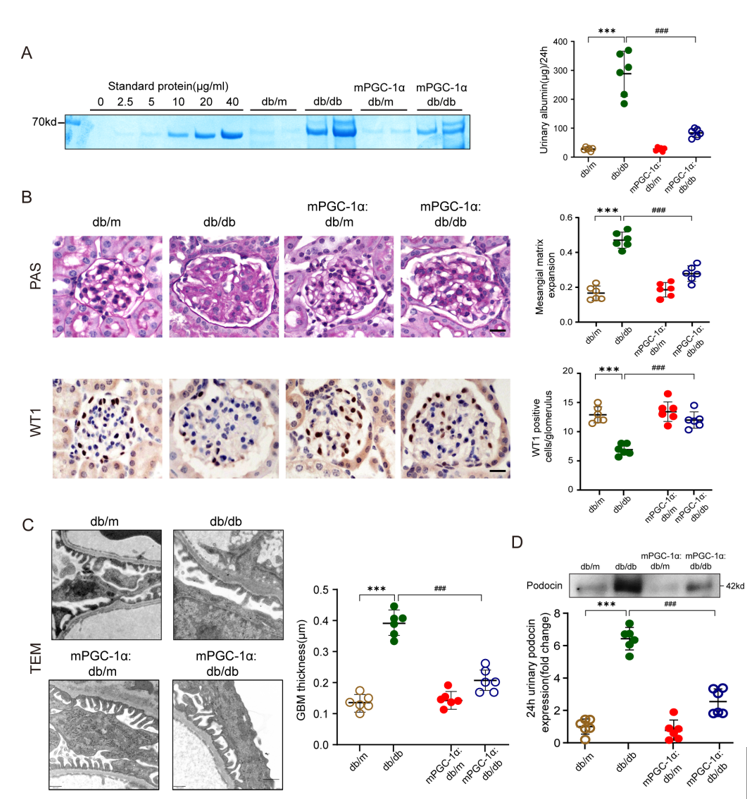
图1. 骨骼肌特异性PGC-1α过表达改善糖尿病肾病小鼠的足细胞损伤。
进一步研究表明,mPGC-1α:db/db小鼠的足细胞较db/db小鼠表达更高的Nephrin和COXIV水平,以及多个线粒体功能相关基因的上调。提示mPGC-1α预防糖尿病小鼠足细胞的线粒体损伤(图2)。
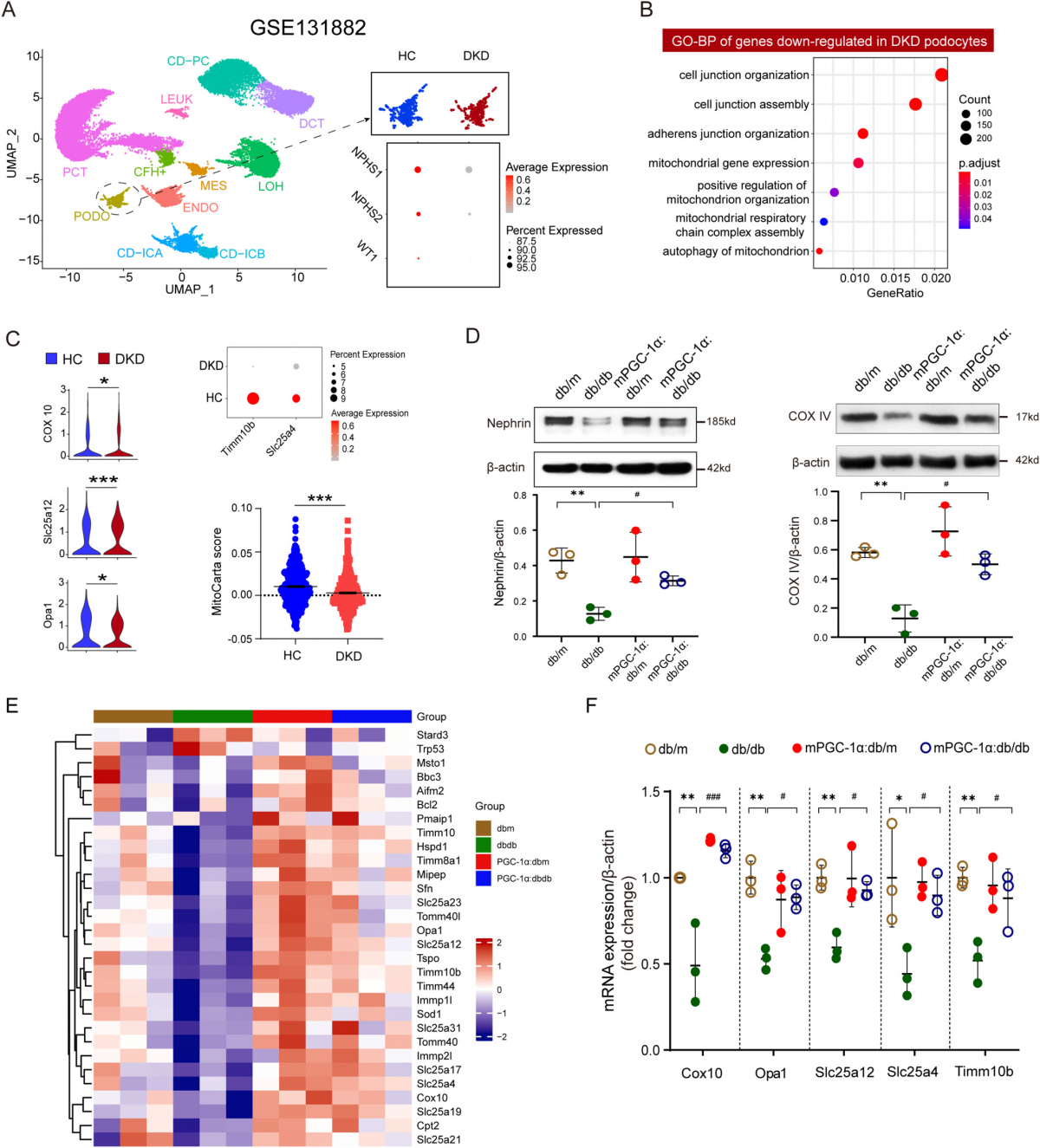
图2. 骨骼肌特异性PGC-1α过表达减轻糖尿病小鼠足细胞的线粒体损伤。
研究团队进一步分析了小鼠肌肉中的肌肉因子表达,发现肌肉中IL-15表达明显增多,血浆中IL-15的浓度也相应增加。同时研究团队通过临床样本分析发现,糖尿病肾病患者的血浆IL-15水平显著低于健康人群,且IL-15水平与尿白蛋白/肌酐比值(UACR)呈负相关(图3)。
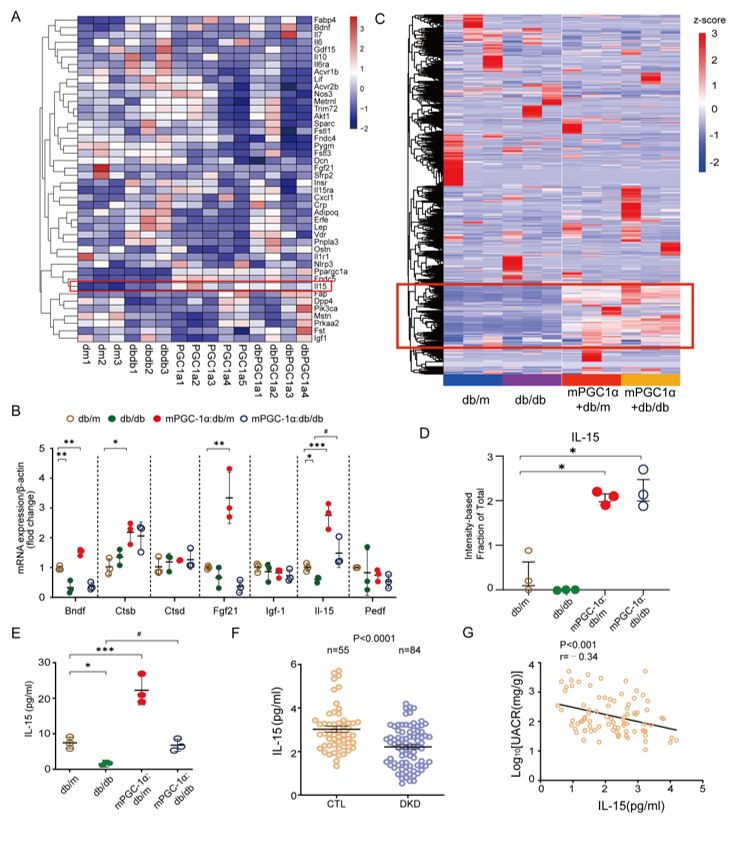
图3. 骨骼肌特异性PGC-1α过表达小鼠中肌肉因子IL-15表达明显增加,且IL-15表现出一定临床意义。
进一步的机制研究揭示,IL-15能显著改善高糖环境下足细胞线粒体功能,提高基础耗氧率、ATP偶联呼吸和最大呼吸能力,减少活性氧(ROS)的产生。该保护作用机制为:在高糖环境下,IL-15通过上调线粒体融合关键蛋白OPA1的表达,维持线粒体的丝状网络形态,抑制异常裂变;而OPA1的表达上调是通过IL-15诱导OPA1启动子区域的组蛋白H3乙酰化实现的表观遗传调控(图4)。
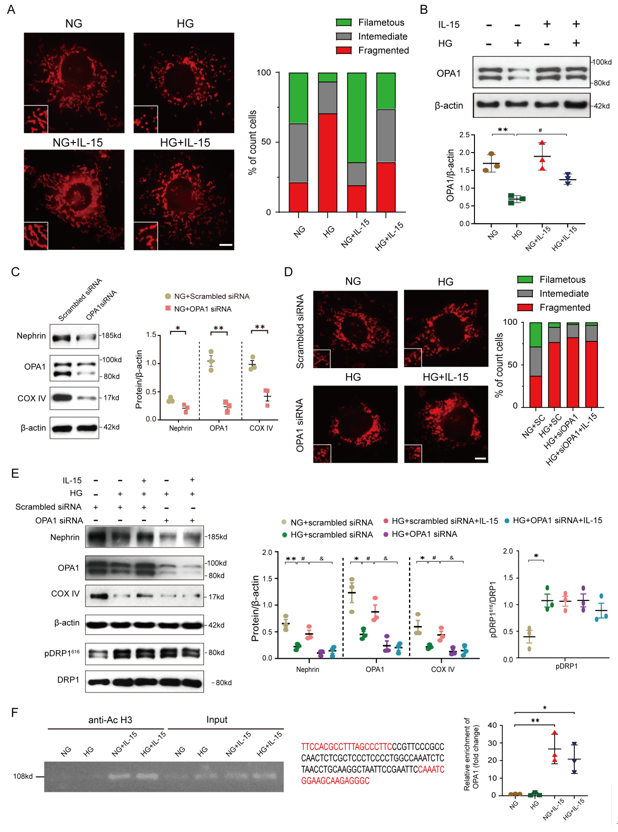
图4. IL-15通过增加OPA1表达维持足细胞线粒体融合减轻高糖损伤。
在治疗潜力验证中,研究团队对db/db小鼠进行重组IL-15腹腔注射,结果显示治疗后小鼠的尿白蛋白排泄量显著降低,系膜基质扩张和肾小球基底膜增厚得到明显改善,足细胞数量得以维持,证实了IL-15作为治疗药物的潜力(图5)。
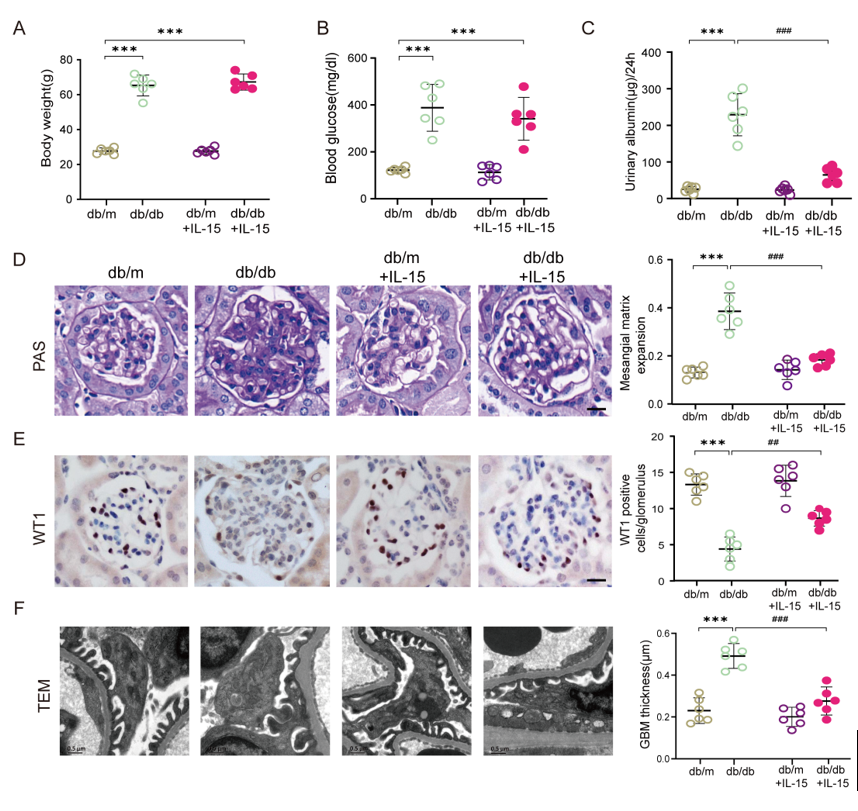
图5. IL-15可以改善糖尿病肾病小鼠的肾脏损伤
综上所述,该研究首次证实骨骼肌来源的IL-15是保护糖尿病肾病的重要肌肉因子,通过表观遗传调控OPA1表达、维持足细胞线粒体融合稳态,从而减轻糖尿病肾病进展。这一发现不仅揭示了肌肉-肾脏对话的新机制,更将IL-15列为糖尿病肾病的潜在治疗靶点,为开发新型靶向治疗策略提供了重要的实验依据和临床思路。
我院肾脏内科李吟副主任医师、饶嘉玲主治医师为该文共同第一作者,彭晖教授和美国贝勒医学院Zhaoyong Hu教授为共同通讯作者。该研究工作得到了国家自然科学基金、广东省企业联合基金重点项目、广州市基础与应用基础研究基金等项目的资助。
原文链接:https://onlinelibrary.wiley.com/doi/10.1002/jcsm.70256









